Ізотопи— це нукліди одного хімічного елемента, які мають однакове протонне число (заряд ядра). Зверни увагу, термін «ізотопи» вживається лише у множині (застаріле «ізотоп» і є нуклід). Наприклад, природний Оксиген, крім нуклідів 16О, містить ще атоми з нуклонними числами 17 і 18.30 лип. 2018 р.
Загалом, існує 254 стабільних ізотопи, що належать 81 елементу, при тому, що загалом відомо 3339 різних ізотопів. З цих ізотопів, теоретично, лише 90 є повністю стабільними, а решта просто має дуже довгі періоди напіврозпаду, проте на практиці їх розпад не спостерігався.
Ізотопи — різновиди атомів з однаковим числом протонів у ядрі (зарядом ядра), але різним числом нейтронів. Отже, ізотопи відрізняються тільки числом нейтронів. Протони визначають властивості атома, тобто надають йому індивідуальність. А нейтрони не впливають на властивості атома, а відображаються на його масі.
Атоми, які мають однакову кількість протонів, а значить і однаковий атомний номер, але різну кількість нейтронів, називаються ізотопами. Всі ізотопи елемента мають однакову кількість протонів і електронів, а значить, вони демонструють однакову хімію.
Атоми одного елемента з різною кількістю нейтронів називаються ізотопами. У центрі атома знаходиться крихітне, позитивно заряджене ядро, що складається з протонів та нейтронів. Ядро атома приблизно в 100 000 разів менше, ніж сам атом.
Нейтрон (позначається n) — електрично нейтральна частинка. Нейтрон стабільний лише у складі стабільних атомних ядер. Вільний нейтрон — нестабільна частинка, яка розпадається на інші частинки. Нуклони — це протони й нейтрони, що входять до складу ядра атома.
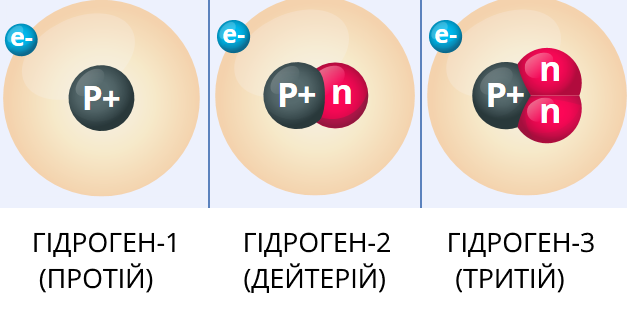
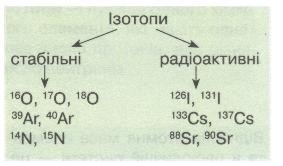
Ізото́пи — нукліди одного і того самого хімічного елементу, які мають різну кількість нейтронів, а, отже, різне масове число і різну атомну масу.